Si habéis leído en el apartado de "Aprendemos 'LA LLEGADA DE LA MEDICINA BASADA EN LA EVIDENCIA. INTRODUCCIÓN AL MUNDO DE LOS ENSAYOS CLÍNICOS' " habéis podido apreciar la necesidad de realizar Ensayos Clínicos (EC) debido a qué son una herramienta indispensable para valora si un tratamiento puede ser considerado como práctica clínica habitual. También hemos visto que para que un tratamiento pueda ser utilizado en un EC, deberemos solicitar el permiso correspondiente una vez realizados los estudios preclínicos adecuados.

Un Ensayo o Estudio clínico se define como toda investigación efectuada en seres humanos dirigida a determinar o verificar los efectos clínicos, farmacológicos y/o demás efectos farmacodinámicos, y/o identificar cualquier reacción adversa, y/o estudiar la absorción, distribución, metabolismo y excreción de uno o varios medicamentos en investigación con el propósito de determinar su seguridad y/o eficacia (guías ICH-GCP).
Los ensayos clínicos son experimentos y requieren la correcta aplicación de diseños experimentales: una hipótesis, unos objetivos, un plan detallado de aplicación, un análisis de resultados; unas herramientas para controlar el error sistemático (sesgo), reducir el error producido por el azar, incrementar la precisión y evaluar las interacciones de los tratamientos.
Aunque el tipo de ensayo que tiene valor decisivo es el randomizado que compara dos tratamientos, existen unos pasos previos hasta llegar a él, ya que no se podría administrar un nuevo tratamiento a nadie sin tener unos datos básicos de seguridad y eficacia. Estos estudios previos se llaman estudios en fase I y II.
Como vemos, los ensayos clínicos se denominan de maneras diferentes según su INTENCIÓN:
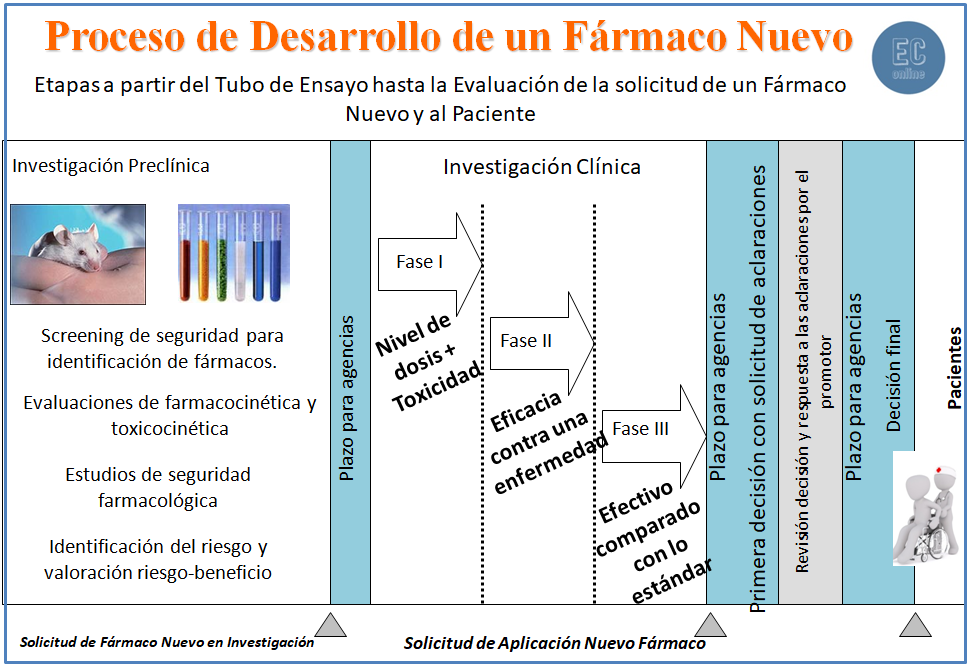
• Los estudios que buscan la dosis a administrar en humanos, la toxicidad e información de lo que la droga hace al organismo y el organismo hace a la droga, se llaman estudios de fase I.
• Los estudios que buscan los datos imprescindibles de eficacia del tratamiento para decidir seguir o no con la investigación de dicho tratamiento, se llaman de fase II.
• Los estudios que pretenden comparar el nuevo tratamiento contra el fármaco estándar o frente la historia natural de una enfermedad y demostrar que es más efectivo, se llaman de fase III.
• Se denominan fase IV. los estudios que se realizan después de la comercialización de un producto o medicamento y pueden tener intenciones y circunstancias diversas. Nos solemos referir a ellos como: fase IV/II ó IV/III, según, obviamente, su intención.
Analizamos cada una de las fases: